Beton. Stavební materiál, bez kterého se neobejde téměř žádná stavba
Beton je kompozitní stavební materiál. Vzniká smícháním sypkého pojiva, plniva, přísad a příměsí ve vodné suspenzi, připomínající tvárnou kaši. Po ztuhnutí pojiva vznikne pevný slepenec. Nejčastějším betonem je cementový beton, v němž je pojivem cement a plnivem kamenivo.
Výše uvedená definice se v širším významu týká nejen betonů do podlah, základů, litých konstrukcí apod., ale i zdicích malt, omítek a dalších. Právě tak budeme chápat pojem beton i v tomto pojednání.

Historie cihly od neolytu přes Babylon až po současnost
Objevení hlíny, rozvoj pecí pro její vypálení, představení glazování a způsoby tvarování cihel do forem sochařství, rozdělení profese mezi cihlářem a zedníkem a rozvoj…
Nejčastější pojiva
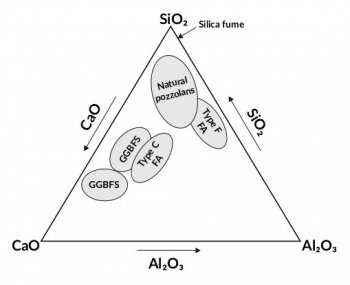
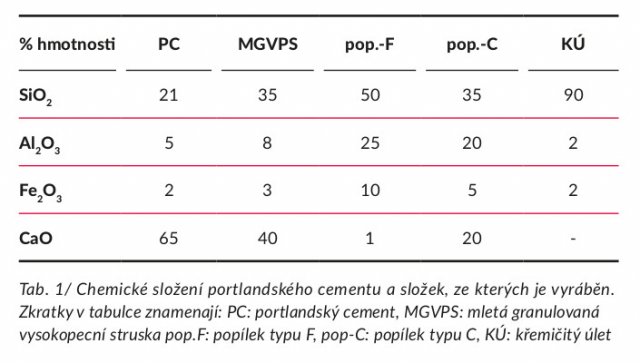
Nejznámějším pojivem v České republice je zřejmě portlandský cement. K jeho výrobě je zapotřebí zejména mletá granulovaná vysokopecní struska (MGVPS), elektrárenský popílek typu F (pop.-F) a C (pop.-C) a křemičitý úlet (KÚ), jejichž zastoupení v portlandském cementu (PC) znázorňují příslušné bleděmodré plochy v ternárním diagramu na obr. 2. V blízkosti vrcholů trojúhelníka je křemen (SiO2), korund (Al2O3) nebo hematit, česky krevel (Fe2O3) a v posledním vrcholu je pálené vápno (CaO) nebo periklas (MgO).
Každý bod ternárního diagramu představuje určitý typ cementu. Příkladem je pucolánový popel, vlastně jemný písečný sopečný popel, který byl využíván od starověku jako hydraulické pojivo do malt a betonů. Chemicky je to vulkanic ký hlinitokřemičitan, který byl objeven již v dobách starého Říma u města Pozzuoli na úbočí Vesuvu (Itálie) a později i jinde. Stavby, kde byl tento cement použit jsou např. římské Koloseum, Pantheon a jiné.
Popílek, používaný přivýrobě dnešního cementu, je anorganická zplodina vznikající při spalování pevných, zpravidla jemně mletých paliv v uhelných elektrárnách. Zachycuje se z kouřových plynů v mechanických a elektrických odlučovačích. Při výrobě betonu se jedná o latentně hydraulickou příměs.
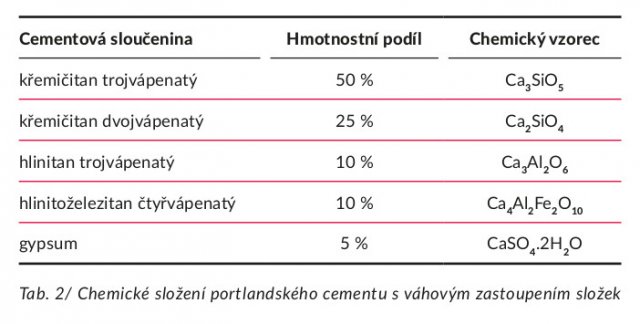
Přidáme-li do cementu vodu, každá ze sloučenin v tab. 1 podstoupí hydrataci a přispěje tím k výsledné kvalitě betonu. Pouze křemičitany vápníku přispívají k pevnosti. Křemičitan trojvápenatý je odpovědný za velkou část počátečního ztvrdnutí (prvních 7 dní). Křemičitan dvojvápenatý, který reaguje pomaleji, přispívá jen k pevnosti v pozdější době.
Rovnici hydratace křemičitanu trojvápenatého v betonu lze zapsat jako:
2 Ca3SiO5 + 7 H2O → 3 CaO·2SiO3·4H2O + 3 Ca(OH)2 + 173,6 kJ
Na přidání vody reaguje tento křemičitan uvolňováním vápenatých iontů Ca2+, hydroxylových iontů OH– a velkého množství tepla. Také pH rychle roste k hodnotě nad 12 (kvůli OH–). Intenzita této počáteční hydrolýzy však rychle klesá a s tím i uvolňované teplo.
Později pak dochází k tomu, že začíná pomalu krystalizovat hydroxid vápenatý a s ním i dvojkřemičitan vápenatý. Ionty tvoří sraženinu, což dál urychluje rozklad křemičitanu trojvápenatého na vápenaté a hydroxylové ionty (podle zákona akce a reakce). Přitom se opět uvolňuje teplo.
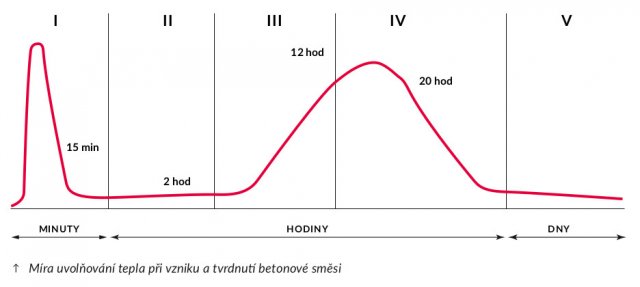
Takto se vysvětluje vznik dvou teplotních maxim, které po namíchání čerstvého betonu doprovázejí reakce (hydrataci a krystalizaci) vedoucí k jeho ztvrdnutí. Lze také říci, že pevné chemické vazby ve vápenci a křemeni, které byly rozbity žárem rotační pece při výrobě slínku, se v betonu obnovují, beton tím tvrdne a původně dodané teplo se uvolňuje.
Další používaná pojiva
Sádra a anhydrit. Kromě cementu známe i další pojiva. Je to zejména anhydrit nebo sádra, mluvíme také o anhydritových nebo sádrových betonech či omítkách. Surovinou je v obou případech přírodní nebo elektrárenský sádrovec o chemickém složení CaSO4·2H2O, tedy dihydrát síranu vápenatého, který lze tepelně převést na sádru – hemihydrát CaSO4·1⁄2H2O nebo bezvodý anhydrit CaSO4, který existuje ve třech krystalografických modifikacích I, II a III. Dehydratace sádrovce probíhá v těchto fázích:
- teplota 95 až 130 °C – sádrovec → hemihydrát
- teplota 150 až 230 °C – hemihydrát → A III
- teplota 400 až700 °CA – III → A II
- teplota 800 °C – A II → A I
Chemicky stabilní jsou jen sádrovec a anhydrit II. Pojivovým materiálem, který se aktivuje přidáním vody, je pak hemihydrát nebo směsi hemihydrátu a anhydritu I a III. Asi nejznámější je sádra na bázi hemihydrátu, která po smíchání s vodou velmi rychle tvrdne při uvolnění velkého množství tepla, což snadno zaznamenáme dotykem. Opět se uvolňuje teplo, které se spotřebovalo k rozkladu sádrovce, podobně jako bylo u cementu. Ohřátí tuhnoucí sádry je nápadné proto, že probíhá v řádu minut, zatímco beton tvrdne v řádu dní.
Sorelův cement je méně známý. Připravuje se smícháním práškového oxidu hořečnatého MgO (magnezitu) s vodním roztokem chloridu hořečnatého, MgCl2. Tím vzniká sloučenina 5Mg(OH)2·MgCl2·7H2O. Místo magnezitu lze použít i pálený dolomit, který ale musí být vypálen při nižší teplotě, aby se nerozložila jeho vápencová složka, protože oxid vápenatý (CaO) zhoršuje vlastnosti pojiva, zejména odolnost proti vlhkosti. Sorelův cement vyniká pevností, odolností proti vlhkosti, objemovou stálostí a dobrou afinitou k organickým materiálům, u nichž navíc výrazně zvyšuje požární odolnost. Nevýhodou je jeho chemická agresivita vůči kovům, zejména oceli, na níž způsobuje intenzivní korozi. Využívá se jako pojivo pro desky s organickým plnivem, například heraklitové desky. Dříve se používal pro přípravu malty a stavebních tmelů.
Hašené vápno řadíme také mezi pojiva. Jde o čistý hydroxid vápenatý Ca(OH)2, který dostaneme žíháním (kalcinací) vápence CaCO3 při teplotách nad 825°C podle rovnice:
CaCO3 + teplo → CaO + CO2
Vzniklý oxid vápenatý CaO sa pak „hasí“vodou podle rovnice:
CaO + H2O → Ca(OH)2
K hašení se při výrobě použije právě tolik vody, aby reakce proběhla úplně a nepřebýval ani oxid vápenatý ani voda. Vzniklé hašené vápno Ca(OH)2 je tak suché a lze ho pytlovat a expedovat.
Hydraulické vápno je pojivo jiného druhu. Vzniká kalcinací vápence znečištěného jílem. Jílovité nečistoty obsahují křemičitany, které způsobují hydrauličnost vápna, což je schopnost „tvrdnout i pod vodou“, přesněji za nepřístupu vzduchu. Vedle toho také urychlují tvrdnutí.
Asfaltový beton je název pro materiál vrchní krytové vrstvy silnic, dálnic a jiných pojížděných povrchů. Základní charakteristikou je použití asfaltu jako pojiva pro kamenivo. Pojivo při vysoké teplotě zajistí stmelení zrn kameniva, po položení, uválcování a vychladnutí je možno vrstvu užívat. Ohřátím lze vrstvu znovu zpracovat.
Beton a životní prostředí
Podrobný pohled na problematiku vlivu různých lidských činností na životní prostředí ukazuje, že výroba cementu patří k vůbec nejčistším lidským aktivitám. Srovnávacím kritériem může být tzv. emisní faktor, což je emise, která vznikne při spalování např. jedné tuny paliva a vyjadřuje se v gramech škodliviny na tunu spáleného paliva. Odvětví výroby cementu lze takto porovnat například s elektrárenstvím, strojírenstvím, dopravou, zemědělstvím, potravinářství nebo provozem domácností.
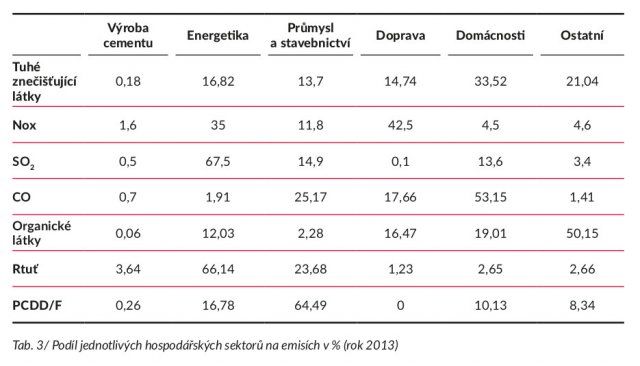
Jiným kritériem je podíl daného hospodářského odvětví, v našem případě cementářství, na celkovém znečištění danou škodlivinou či souhrnem škodlivin viz tab. 3.
Skleníkový efekt
Při výrobě cementu uniká do ovzduší množství oxidu uhličitého CO2 v důsledku kalcinace vápence CaCO3 nebo dolomitu CaMg(CO3)2. To samozřejmě vyvolává otázku nad klimatickou změnou. Otázku, která je často umocňována tím, že se stalo z ochrany klimatu politikum, jež mnohdy vylučuje'věcnou diskusi a hledání správných řešení. Pohledů na klimatickou změnu či globální oteplování a oxid uhličitý je však více.
V časopisu Stavebnictví a interiér jsem kdysi uvedl: „Biliony dolarů, které politici po světě vysbírali od daňových poplatníků a vložili do dokazování globálního oteplování, byly utraceny, ale žádný důkaz se nekonal. Nikdo neobdržel Nobelovu cenu a nevznikl ani fyzikální model, který by globální oteplování rozumně předpověděl a navrhl řešení, jak se mu vyhnout. Nalézt však lze fakta, která vliv emisí CO2 na globální oteplování vyvracejí. Fakta, která ukazují, že přiléváním skleníkového plynu do atmosféry se zmenšuje její schopnost izolovat.“
Molekuly skleníkových plynů totiž tepelné záření od Země neodrážejí. Odrážet může jen souvislý lesklý kovový povrch, což atmosféra není. Zemské sálání tak mohou skleníkové plyny pouze pohltit a takto získanou energii následně předávat okolním molekulám (zejména kyslíku O2 a dusíku N2) nebo ji vyzařovat dolů k Zemi a do vesmíru. Toto vyzařování je ale úplně jiné, než to zemské. Zejména má mnohem nižší teplotu (hluboko pod 0 °C), takže na Zemi působí spíš chladivě.
Jinými slovy: skleníkové plyny, mezi které patří i CO2 a jenž vzniká při výrobě cementu, vytvářejí teplotu atmosféry ve vyšších vrstvách vysílající k Zemi vlastní tepelné záření o nízké teplotě, působící chladivě. Sálají i opačným směrem do vesmíru, což je nekonečný prostor o teplotě cca –270 °C. Lze tedy říci, že skleníkové plyny vytvářejí kolem Země sálavou vrstvu, která Zemi chrání před působením chladného vesmíru a která zároveň „umí“ odsálat velké množství energie rovnou do vesmíru, včetně energie skupenského tepla vodní páry odpařované z oceánů. Což kyslík a dusík nedokáží. Tím jsou vyšší vrstvy troposféry a celá planeta účinně chlazeny na stabilizované teplotní hladině.
V zásadě se tak není třeba bát ani toho ,kdyby se průmysl „utrhl z řetězu“ a spálil veškerá ložiska uhlí, vytěžil všechny vápence a dolomity a všechen v nich vázaný uhlík vpustil v podobě CO2 do atmosféry. Následkem by totiž bylo pouze to, že bychom se octli v podmínkách, jaké tu byly, když začal na planetě rašit život. V atmosféře by byl zhruba dvakrát vyšší obsah oxidu uhličitého a kyslíku asi o dvě procenta méně než dnes. To bezpečně zvládá jak člověk, tak i živočichové zde žijící.
Literatura a zdroje
- "The History of Concrete". Dept. of Materials Science and Engineering, University of Illinois, Urbana-Champaign. Načteno 1. února 2017.
- http://matse1.matse.illinois.edu/concrete/hist.html. Načteno 1. února 2017.
- Kotlík Petr a kol.: Stavební materiály historických objektů. Vydala VŠCHT Praha v roce 1999.
- Otakar Kallauner: Sorelův cement, jeho výroba, vlastnosti a užití. 1912 Praha
- Jiří Hejhálek: Zemské klima. Problém, který neexistuje. Stavebnictví a interiér 11/2016, str. 41, www.stavebnictvi3000.cz
- Jiří Hejhálek: Tepelné záření a navrhování reflexních fólií do staveb, Vega společnost s ručením omezeným, 2014.